LA THYROÏDE – (et la nutrition)
200 millions de personnes dans le monde souffriraient de la thyroïde. C’est une pathologie fréquente en France puisqu’elle touche 1 à 2 % de la population. Parmi elles, 90% souffrent d’hypothyroïdie et 10% d’hyperthyroïdie. Ce sont les femmes, et particulièrement les plus âgées d’entre elles, qui sont le plus atteintes.
La thyroïde gère des aspects vitaux de notre santé : croissance, humeur, transit, régulation de la température corporelle, cholestérol, glycémie, rythme cardiaque et bien d’autres.
On peut considérer la thyroïde comme étant la boite de vitesse d’un véhicule sophistiqué. Si la boite de vitesse est endommagée, c’est le moteur dans son ensemble qui fait défaut. En d’autres termes, un déficit en hormones thyroïdiennes n’est pas compatible avec une santé normale. Au-delà de l’inconfort quotidien, une thyroïde déficiente peut donc finir par conduire à des conséquences médicales graves comme un surpoids persistant avec risque de diabète de type 2, une fragilité cardiaque, une impossibilité à tomber enceinte, perturber et « enrailler » de grands systèmes.
Le fonctionnement thyroïdien passe par plusieurs mécanismes : le cycle débute au niveau du système nerveux central, puis de l’hypothalamus, puis de l’hypophyse vers la thyroïde, de la thyroïde vers le foie et les intestins, ensuite vers le plasma, et pour terminer dans nos cellules. Durant ce périple, notre corps a besoin de différents macronutriments (la L-Tyrosine), micronutriments (Zinc, Sélénium, Fer, Iode, Magnésium), vitamines (A,B,C,D,E) dits cofacteurs, qui ont chacun leur importance. Les carences sont susceptibles d’empêcher tous ces mécanismes de fonctionner correctement.
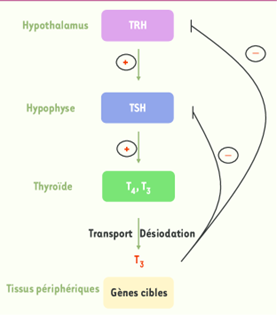
L’axe hypothalo-hypohyso-thyroïdien
L’hypothalamus sécrète de la TRH (thyrotropin-releasing hormone) qui va stimuler la libération de TSH (thyroid-stimulating hormone) par l’antéhypophyse. La TSH va se fixer sur un récepteur présent sur la thyroïde et provoquer la synthèse d’hormones thyroïdiennes.
La plupart des systèmes hormonaux sont contrôlés par un système de rétroaction. Ainsi, en retour, les hormones thyroïdiennes circulantes agissent sur l’hypophyse et sur l’hypothalamus. Elles suppriment la production de TSH et de TRH, et diminuent donc la sécrétion des hormones thyroïdiennes. Il s’agit là d’un processus de « rétroaction négative », qui représente le mécanisme le plus commun de régulation des taux circulants d’hormone. Inversement, une chute de la sécrétion des hormones thyroïdiennes (par exemple après thyroïdectomie) conduit à une sécrétion accrue de TSH et de TRH. Ce rétrocontrôle se fait principalement d’après la concentration en hormone t4.
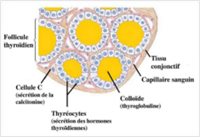
Anatomie de la thyroïde
Elle est située à la base du cou, juste sous la peau et avant de la trachée. Son nom issu du grec signifie « le bouclier ». Aujourd’hui on la compare souvent à un papillon. Elle se compose de deux parties nommées lobes reliées par un isthme prolongé verticalement en général par une partie fine que l’on appelle « la pyramide de l’alouette ». Le tissu thyroïdien est constitué des thyréocytes (à 99%, le reste étant les cellules C à l’origine de la production de calcitonine). Ces thyréocytes se répartissent en cercle (en boule en 3D) autour d’une substante pâteuse jaune appelée colloïde, remplie de thyroglobuline (protéine précurseur des hormones thyroïdiennes). L’ensemble thyréocyte et colloïde forme le follicule thyroïdien.
Fonctionnement physiologique et rôle de la thyroïde
La thyroïde est le régulateur central de notre organisme. Elle libère dans le sang des messagers, les hormones thyroïdiennes capables d’agir sur l’ensemble des cellules de l’organisme. La multiplicité des actions et des organes cibles des hormones thyroïdiennes est illustrée par la richesse de la symptomatologie de l’hyperthyroïdie comme de l’hypothyroïdie quand elles ont une forme sévère. Voici quelques fonctions de la glande thyroïde (liste non exhaustive) :
Les hormones thyroïdiennes augmentent la consommation d’oxygène et la thermogenèse : le métabolisme basal est plus élevé. La lipogenèse et la lipolyse sont sous la dépendance du fonctionnement de la thyroïde. On constate qu’une augmentation des hormones thyroïdiennes diminue les concentrations sanguines de LDL et de cholestérol. La synthèse hépatique du cholestérol est stimulée, mais la dégradation de celui-ci l’est plus encore. L’hyperthyroïdie provoque une augmentation de la production de glucose et de son utilisation ayant pour conséquence une glycosurie et une hyperglycémie postprandiale excessive en cas de surplus d’hormones thyroïdiennes.
Sur le métabolisme des protéines, on observe qu’à doses physiologiques, les hormones thyroïdiennes sont anabolisantes. Cependant, à doses trop élevées, elles ont un effet catabolisant.
Sur les os et le squelette : action sur la synthèse et la destruction osseuse, la destruction étant quand même un peu plus active que la synthèse. (Par conséquent, une ostéoporose peut apparaître dans les hyperthyroïdies, réversible au retour à l’euthyroïdie).
Sur les muscles et notamment sur le cœur : action sur les protéines musculaires, en particulier la myosine. Au niveau cardiaque, les hormones ont un effet chronotrope (augmentent la fréquence cardiaque), ionotrope (augmentent la force de contraction), et dromotrope (facilitent la vitesse de conduction). Les muscles lisses sont également concernés, comme ceux impliqués dans la motilité intestinale : une augmentation du métabolisme thyroïdien les stimule, accélérant le transit jusqu’à provoquer une diarrhée ou une constipation dans le cas inverse.
Sur le système nerveux : Les hormones thyroïdiennes jouent un rôle important dans le développement et la maturation du système nerveux. Une carence à la naissance ou pendant les premières années de vie peut conduire à un retard mental plus ou moins important. Chez l’adulte, un manque d’hormones va ralentir l’intellect, le sujet devient léthargique. Au contraire, un sujet qui reçoit un excès d’hormones thyroïdiennes est hyper-irritable et réagit excessivement à son environnement.
Et enfin sur le système reproducteur : La thyroïde intervient dans le déroulement de la puberté, une hypothyroïdie peut être responsable d’un retard. Chez l’adulte, un dysfonctionnement thyroïdien perturbe la fertilité et la sexualité.
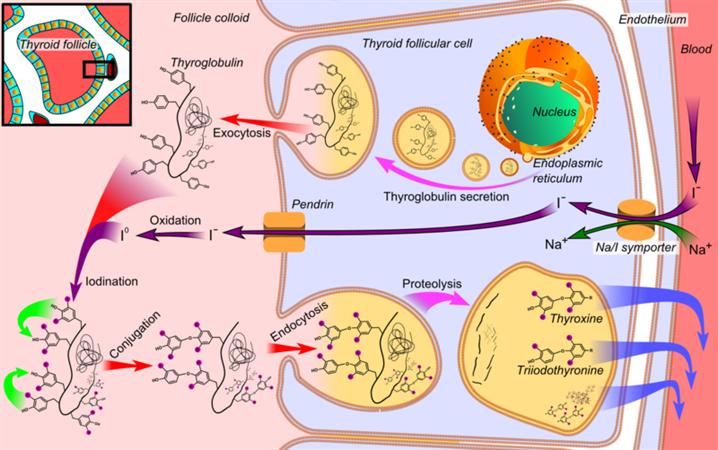
Processus de fabrication des hormones thyroïdiennes
La synthèse des hormones thyroïdiennes nécessite de l’iode. L’iode, ingéré dans les aliments et l’eau sous forme d’iodure, est activement concentré par la thyroïde et converti en iode organique (organification) dans les cellules folliculaires par la Thyroperoxydase thyroïdienne (TPO). Cette oxydation est ordonnée par la TSH sécrétée par l’hypophyse.
Nb : Par définition, une peroxydase nécessite la présence d’H2O2 (eau oxygénée) pour assurer sa fonction oxydative. Cette transformation/oxydation est donc fortement oxydante.
La thyroglobuline et les ions iodures se retrouvent ensuite dans le colloïde. L’iodation des résidus de tyrosine présents dans la thyroglobuline aboutit à la formation de mono- ou di iodotyrosines (MIT ou DIT > t1 et t2) selon le nombre d’atomes d’iode fixés sur le résidu. La thyroperoxydase (TSH) catalyse également le couplage des iodotyrosines entre elles pour former des iodothyronines : ce sont la triiodothyronine (t3) ou tétra-iodothyronine (t4 ou thyroxine) ou encore la t3-reverse ou r-t3, hormone inactive. (Son rôle est d’éliminer la t4 de l’organisme et d’éviter un excès de t3.
- Diiodotyrosine (t2) + diiodotyrosine (t2) → t4 (Tétraïodothyronine ou thyroxine)
- Diiodotyrosine (t2) + monoïodotyrosine (t1) → t3 (Triiodothyronine)
T4 et t3 restent incorporées dans la thyroglobuline au sein du follicule jusqu’à ce que les cellules folliculaires captent la thyroglobuline sous la forme de gouttelettes de colloïde. Une fois à l’intérieur des cellules folliculaires thyroïdiennes, la thyroglobuline repasse dans les thyréocytes par endocytose pour rejoindre les lysosomes (organites cellulaires).
Les lysosomes séparent les t3 et les t4 de la thyroglobuline par des enzymes lysosomales. Elles sont ensuite libérées dans la circulation sanguine, où elles sont liées à des protéines sériques de transport. La protéine de transport primaire est la globuline liant la thyroxine (thyroxine-binding globulin, TBG), qui a une grande affinité mais une faible capacité de transport de t3 et de t4. La TBG transporte habituellement environ 75% des hormones thyroïdiennes liées.
Ces hormones agissent ensuite sur les cellules dans presque tous les tissus du corps en se liant à des récepteurs nucléaires et en modifiant l’expression d’un large éventail de produits de gènes. La t3 est la forme qui se lie le plus activement au récepteur nucléaire (forme active) ; la t4 n’a qu’une activité hormonale minime. Cependant, la t4 a une durée de vie plus longue (7 jours) et peut être convertie en t3 (durée de vie plus courte de 24h) dans la plupart des tissus mais essentiellement dans le foie et sert ainsi de réservoir ou de pro hormone pour la t3. Une 3ème forme d’hormone thyroïdienne, la t3 reverse (rt3), qui n’a pas d’activité métabolique, est produite par la thyroïde. La t3 reverse sert de réserve pour le corps en t3 dormantes, qui pourront être utilisées en cas de besoin. Le corps produit en permanence une combinaison d’hormones t3 actives et t3 reverse, c’est un processus naturel et normal mais la quantité de ces deux hormones doit rester équilibrée l’une par rapport à l’autre pour ne pas poser de problème. (Un excès de rt3 peut avoir lieu en cas de pathologie hépatique, infections, jeûne ou stress).
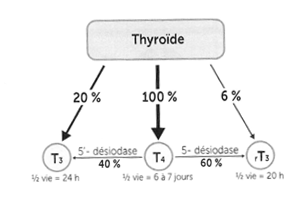
La thyroïde synthétise 100 % de la t4 mais seulement 20% de la t3 et 6% de rt3. Ces deux dernières proviennent essentiellement de la transformation périphérique de la t4. Pour devenir t3, la t4 (précurseur de la t3), doit donc perdre un atome d’iode. Cette conversion se passe essentiellement dans le foie, dans les reins mais également de façon moindre dans d’autres organes (cœur, muscles, cerveau, tube digestif) grâce à une enzyme qui contient du sélénium, la désiodase. On parle de réaction de désiodation. 20% de la t4 est transformée en t3 dans l’intestin grâce à l’enzyme sulfatase intestinale synthétisée par les bactéries saines du microbiote. Il existe deux types de désiodases dans le métabolisme des hormones thyroïdiennes : la 5’-désiodase qui transforme la t4 en t3 active et la 5-désiodase qui transforme, elle, la t4 en rt3 (t3 reverse).
Zoom sur l’enzyme désiodase : certains cofacteurs sont essentiels pour que la 5’-désiodase fonctionne. Il faut de l’iode, du magnésium, du zinc, du sélénium, du molybdène (rare carence), du fer, du cuivre (rare carence), de la vitamine A, B6, B9. D’autres facteurs peuvent être à l’origine d’une augmentation de t3 reverse en privilégiant la voie de la 5 -désiodase tels que le stress chronique, les restrictions caloriques, un jeûne prolongé et régulier, les maladies infectieuses, une insuffisance hépatique, des déficits en minéraux, vitamines, oligo-éléments, le syndrome de Cushing (hypercortisolisme) ou encore une forte exposition aux métaux lourds.
L’hypothyroïdie
L’hypothyroïdie est un dérèglement de la glande thyroïde qui ne secrète plus assez d’hormones thyroïdiennes (3 à 10 % des Français).
La maladie de Hashimoto est la cause la plus fréquente d’hypothyroïdie (thyroïde sous-active). C’est un trouble auto-immunitaire où le système immunitaire crée des anticorps anti-thyroperoxydase (anti-TPO), ou anti-thyroglobuline (anti-TG) qui attaquent les cellules de la glande thyroïde. Cela provoque une inflammation et altère la capacité de la glande thyroïde à produire des hormones thyroïdiennes, conduisant à l’hypothyroïdie. Dans certains cas très rares, Hashimoto peut également provoquer des symptômes d’hyperthyroïdie (souvent dans le début de la maladie, on observe une phase d’hyperthyroïdie). L’hypothyroïdie peut également être iatrogène, provoquée par une radiothérapie anticancéreuse au niveau du cou ou de la poitrine (qui endommage la thyroïde), ou par la prise de certains médicaments : le lithium (utilisé dans le traitement des troubles bipolaires), l’interféron (utilisé pour traiter les hépatites virales, la sclérose en plaques, etc.) ou l’amiodarone (utilisé dans le traitement de certains troubles cardiaques). Le plus souvent, ces médicaments provoquent des hypothyroïdies sans symptômes.
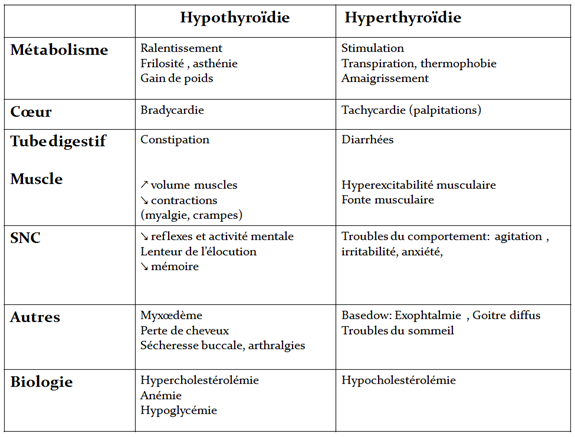
Les signes cliniques caractéristiques de l’hypothyroïdie
- Frilosité+++, extrémités froides, fatigue+++ (surtout le matin au réveil), prise de poids et difficulté à en perdre malgré des restrictions caloriques, hypotension ou hypertension, hypercholestérolémie, infections fréquentes (notamment troubles ORL à répétions), ongles fragiles (mous,fins) , cheveux cassant et secs, diminution de la queue du sourcil (signe d’Hertoghe), peau sèche et pâle, dépression, constipation+++, diarrhées, dysbiose, faiblesse hépatique, difficultés à digérer les graisses, reflux gastriques, calculs biliaires, baisse de la libido, visage gonflé (surtout au réveil), paupières gonflées, poches sous les yeux, jambes lourdes et mauvaise circulation, voix rauque, brouillard mental, somnolence, problèmes de mémoire, altération du cycle menstruel, infertilité, douleurs articulaires, crampes, (parfois insomnies, tremblements)…..>>>> ralentissement général du système et du métabolisme !!!
Les principaux cofacteurs essentiels de la thyroïde
La L-tyrosine est un élément essentiel de la synthèse des hormones thyroïdienne. Il n’y a en général aucun risque de carence.
- L’iode (synthèse des hormones thyroïdiennes) > sel iodé, algues, poissons, huitres, œufs > 150 µg/j adultes > Femme enceinte = 200 µg
- Le Fer (co-facteur de la TPO) > viandes, foie, boudin, poissons, œufs, lentilles, épinards, persil > 11 à 16 mg/j adultes
- Le Zinc (conversion de t4 en t3) > huitres, foie, viandes, poissons, fruits de mer, noix de cajou, champignons > 7 à 14 mg/j selon l’âge > en complémentation pour combler une carence : entre 15 et 30 mg/j
- Le Sélénium (conversion de la t4 en t3) > fruits de mer, poissons, viandes, foie, œufs, noix du Brésil > 70 µg/J adultes
- Le Magnésium (conversion de t4 en t3) > cacao, sardines, amandes, fruits de mer, céréales, légumes verts > 400 mg/j adultes
- Les vitamines A, vitamines du groupe B (B1,B2,B3,B6,B9,B12), C, D, E (antioxydantes et utilisation de la t3 par la cellule) > fruits, légumes, foie, huile de foie de morue, beurre cru, céréales, poissons, viandes, produits de la mer, huiles vierges crues,….
- La vitamine D > norme santé > doit se située au dessus de 70 ng/ml > complémentation en D3 plutôt qu’en D2 (plus efficace)
| TABLEAU DE SYNTHÈSE | |||
| Élément | Rôle thyroïdien | Recommandations | Sources principales |
| Tyrosine | Synthèse des hormones thyroïdiennes t4, t3 et rt3 Précurseur de la TPO Entre dans la composition de la TSH Précurseur des catécholamines qui influencent la TSH | 39 mg/kg/j chez l’adulte | Protéines animales+++ Légumineuses |
| Iode | Synthèse des hormones thyroïdiennes t4, t3 et rt3 Fait partie de la structure de tous les récepteurs hormonaux | 150 µg/j pour les adultes | Produits de la mer (algues +++), sel iodé, œufs |
| Fer | Nécessaire à la synthèse de la tyrosine depuis la phénylalanine Cofacteur de l’activité de la TPO (férodépendante) Cofacteur de la Désiodase (conversion t4 en t3) Influence le taux sanguin de TSH Nécessaire à l’utilisation de la t3 à l’intérieur de la cellule Carence diminue l’efficacité de la complémentation en iode | Hommes > 11mg/j Femmes > 16 mg/j | Viandes, foie, œufs, légumineuses, herbes et épices |
| Sélénium | Synthèse des hormones t4, t3 et rt3 (un déficit ↑ production rt3) Elément de la Désiodase (conversion t4 en t3) Protège des dommages oxydatifs (cofacteur du GPX) Freine les anticorps anti-TPO Améliore le recyclage de l’iode | 70 µg/j pour les adultes | Noix du Brésil+++, fruits de mer, viandes, poissons, foie |
| Zinc | Synthèse et activité de la TRH Synthèse et libération de la TSH Cofacteur de la Désiodase (conversion t4 en t3) Synthèse des protéines de transport des hormones thyroïdiennes Nécessaire à l’utilisation de la t3 à l’intérieur de la cellule Anti-oxydant | 7 à 14 mg/j selon les tranches d’âges | Viandes, fruits de mer (Huitres+++), jaune d’œuf, oléagineux, foie, produits laitiers |
| Magnésium | Cofacteur de la Désiodase (conversion t4 en t3) Freine les anticorps anti-TPO Augmente l’immunité et diminue les risques de Hashimoto Carence en lien avec les cancers de la thyroïde | Hommes > 380 mg/j Femmes > 300 mg/j | Cacao, sardines, crustacés, oléagineux, céréales, légumes verts et fruits |
| Cuivre | Carence affecte l’axe HHT et donc la production des HT Cofacteur de la Désiodase (conversion t4 en t3) | Hyper rare en France (Étude INCA 2) Hommes > 1,9 mg/j Femmes > 1,5 mg/j | Foie, huitres, oléagineux, légumineuses, plantes aromatiques |
| Manganèse | Rôle éventuel dans le métabolisme des HT Anti-oxydant | Pas de carence en France, pas de recommandations | Fruits, légumes, céréales, oléagineux, pignons de pins. |
| Molybdène | Cofacteur de la désiodase (conversion t4 en t3) Détox hépatique Sert à l’absorption du Fer | Pas de carence référencée 95µg/j pour les adultes | Présent dans la plupart des aliments |
| Vitamine A | Augmente l’absorption de l’iode (synergie avec la carence en I) Régule la production de TSH Capacité antioxydante ++ Déficit réduit la conversion de la t4 en t3 Permet à t3 de rentrer dans le noyau de la cellule | Hommes > 750 µg/j Femmes > 650 µg/j | Produits animaux, huile de poissons, beurre, foie pour le rétinol. Légumes et fruits pour le β-carotène |
| Vitamine du Groupe B | Antioxydantes Carences souvent associées à des maladies auto-immunes Lien avec le métabolisme du Fer Rôle dans la méthylation / détox du foie | B2 > 1,6 mg/j pour les adultes B12 > 4 µg/j pour les adultes | Produits animaux, viandes, foie, légumineuses, céréales, levures, plantes aromatiques, bananes. B12 que dans les produits animaux |
| Vitamine C | Antioxydant majeur Absorption du fer non héminique Potentiel rôle sur le cancer de la thyroïde | 110 mg/j pour les adultes | FRUITS et légumes, cassis, agrumes. |
| Vitamine D | Carence = facteur de risque de maladies auto-immunes thyroïdiennes Réduit les anticorps chez Hashimoto Réduit les symptômes de l’hypothyroïdie | 15 µg/j (600 UI) pour les adultes | Poissons gras, huile de poissons, foie, champignons, beurre, viande, œufs |
| Vitamine E | Fonction antioxydante | 10 mg/j > hommes 9 mg/j > femmes | Huiles végétales Huile de germe de blé +++ |
Les principales causes de l’hypothyroïdie
- Pas assez de synthèse hormonale (mauvaise production de t4 et t3) > hypothyroïdie primaire, secondaire ou tertiaire / prise d’un médicament qui inhibe la production hormonale, consommation excessive d’aliments dits goitrigènes (crucifères, soja, patates douces, millet, etc..), contamination importante aux métaux lourds.
- Maladies auto-immunes (hashimoto, basedow) > destruction de la glande.
- Mauvaise conversion de la t4 en t3 > carences nutritionnelles en cofacteurs, fatigue du foie, hépatites, etc.., excès d’œstrogènes, dybiose
- Conversion en rt3 trop importante > stress, obésité, reins et foie fatigués, diabète, insuffisance rénale, jeûne, excès d’alcool, de café, stress chronique+++, aliments ultra-transformés industriels, sucres raffinés, édulcorants, perturbateurs endocriniens, certains médicaments, infections virales à répétition.
- Non utilisation de la t3 par les cellules > carence en vitamines (A et D) et en cortisone (épuisement des surrénales), diabète, obésité, stress, dépression, infections chroniques.
Les principales causes de carences nutritionnelles
- Alimentation pauvre, monotone, industrielle, ultra-transformée
- Mauvaise absorption liée à une porosité intestinale ou une dysbiose
- Intolérances alimentaires
Les principales causes de la maladie d’Hashimoto
- Prédispositions génétiques > plusieurs membres d’une même famille, diabète de type 1, maladie cœliaque
- Carences nutritionnelles > manque d’iode, sélénium, zinc, fer peuvent entrainer une inflammation
- Fluctuations hormonales > grossesse, ménopause
- Leaky gut / hyperperméabilité intestinale / dysbiose > 70% du système immunitaire est situé dans l’intestin
- Intolérances alimentaires > gluten, protéines du lait, etc…> porosité intestinale
- Infections à répétition > mononucléose, herpès, papillomavirus, EBV > sursollicitation du SI
Pourquoi les femmes sont elles plus touchées ? (10 fois plus)
- Forte influence des hormones sexuelles ( œstrogènes et progestérone) sur la t3. L’apparition des œstrogènes à la puberté pourrait influencer l’immunité de la femme.
- Si terrain propice (génétique) + conditions favorables et déclencheurs (carences, mauvaise balance hormonales, perturbateurs endocriniens, stress…) > déclenchement de la maladie auto-immune possible.
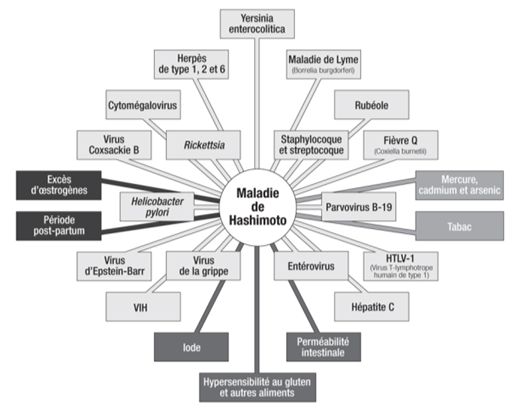
Tirée du livre du Docteur Benoît Claeys – Figure du Docteur Hertoghe